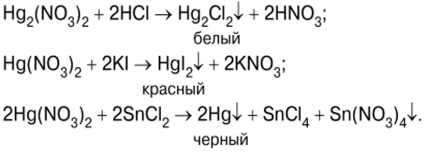
ვერცხლისწყლის ნაერთების რეაქციები
მეტალის ვერცხლისწყალი და მისი ნაერთები ძალიან ტოქსიკურია ცოცხალი ორგანიზმებისთვის. ეს განსაკუთრებით ეხება ნაერთებს, რომლებიც წყალში ძალიან ხსნადია. დიდი სიფრთხილეა საჭირო ამ უნიკალური ელემენტის კომბინაციებზე ექსპერიმენტების დროს (მერკური ერთადერთი ლითონია, რომელიც ოთახის ტემპერატურაზე თხევადია). შეესაბამება ქიმიკოსის ძირითად მითითებებს? საშუალებას მოგცემთ უსაფრთხოდ ჩაატაროთ რამდენიმე ექსპერიმენტი ვერცხლისწყლის ნაერთებთან.
პირველ ექსპერიმენტში ვიღებთ ალუმინის ამალგამს (ამ ლითონის ხსნარი თხევად ვერცხლისწყალში). ვერცხლისწყლის (II) ხსნარი Hg ნიტრატი (V) Hg (NO3)2 და ალუმინის მავთულის ნაჭერი (ფოტო 1). ხსნადი ვერცხლისწყლის მარილის ხსნარით საცდელ მილში მოთავსებულია ალუმინის ჯოხი (ნალექებისგან ფრთხილად გაწმენდილი) (ფოტო 2). გარკვეული პერიოდის შემდეგ, ჩვენ შეგვიძლია დავაკვირდეთ გაზის ბუშტების გათავისუფლებას მავთულის ზედაპირიდან (ფოტო 3 და 4). ხსნარიდან ღეროს ამოღების შემდეგ აღმოჩნდება, რომ თიხა დაფარულია ფუმფულა ფენით და გარდა ამისა, ვხედავთ მეტალის ვერცხლისწყლის ბურთულებსაც (ფოტო 5 და 6).
ქიმია - ვერცხლისწყლის შერწყმის გამოცდილება
ნორმალურ პირობებში, ალუმინის ზედაპირი დაფარულია ალუმინის ოქსიდის მჭიდროდ მორგებული ფენით.2O3ეფექტურად იზოლირებს ლითონს გარემოს აგრესიული გავლენისგან. კვერთხის გაწმენდისა და ვერცხლისწყლის მარილის ხსნარში ჩაძირვის შემდეგ, Hg იონები გადაადგილდებიან.2+ უფრო აქტიური ალუმინი
ღეროს ზედაპირზე დეპონირებული ვერცხლისწყალი ქმნის ამალგამს ალუმინისთან, რაც ართულებს ოქსიდის მასზე შეწებებას. ალუმინი ძალზე აქტიური ლითონია (ის წყალთან რეაქციაში გამოყოფს წყალბადს – შეიმჩნევა გაზის ბუშტები) და მისი სტრუქტურულ მასალად გამოყენება შესაძლებელია მკვრივი ოქსიდის საფარის გამო.
მეორე ექსპერიმენტში ჩვენ აღმოვაჩენთ ამონიუმის NH იონებს.4+ ნესლერის რეაგენტის გამოყენებით (გერმანელი ქიმიკოსი იულიუს ნესლერი იყო პირველი, ვინც გამოიყენა იგი ანალიზში 1856 წელს).
ექსპერიმენტი სვიისა და ვერცხლისწყლის ნაერთების რეაქციაზე
ტესტი იწყება ვერცხლისწყლის(II) იოდიდის HgI დალექვით.2კალიუმის იოდიდის KI და ვერცხლისწყლის (II) ნიტრატის (V) Hg (NO) ხსნარების შერევის შემდეგ3)2 (ფოტო 7):
HgI-ის ნარინჯისფერ-წითელი ნალექი2 (ფოტო 8) შემდეგ დამუშავებული კალიუმის იოდიდის ჭარბი ხსნარით, რათა მივიღოთ K ფორმულის ხსნადი რთული ნაერთი2HgI4 ? კალიუმის ტეტრაიოდერკურატი (II) (ფოტო 9), რომელიც არის ნესლერის რეაგენტი:
შედეგად მიღებული ნაერთით ჩვენ შეგვიძლია ამონიუმის იონების აღმოჩენა. კვლავ საჭირო იქნება ნატრიუმის ჰიდროქსიდის NaOH და ამონიუმის ქლორიდის NH ხსნარები.4Cl (ფოტო 10). ნესლერის რეაგენტში მცირე რაოდენობით ამონიუმის მარილის ხსნარის დამატების შემდეგ და ნიადაგის ძლიერი ფუძით ალკალიზაციის შემდეგ ვაკვირდებით სინჯარის შიგთავსის ყვითელ-ნარინჯისფერი ფერის წარმოქმნას. მიმდინარე რეაქცია შეიძლება დაიწეროს შემდეგნაირად:
მიღებულ ვერცხლისწყლის ნაერთს აქვს რთული სტრუქტურა:
ძალიან მგრძნობიარე ნესლერის ტესტი გამოიყენება წყალში ამონიუმის მარილების ან ამიაკის კვალიც კი (მაგ. ონკანის წყალი).

